現在全世界有超過100種新冠疫苖鬥快推出,據世界衛生組織表示,目前全球有超過30種新冠疫苗進入臨牀試驗階段,其中有9種處於第3期臨牀試驗。美國、英國和中國各有不同疫苖跑在前列,已進入第3期臨床測試。但最新消息是英國牛津大學詹納研究所(Jenner Institute)的疫苖測試時出現問題,要馬上暫停。
英國牛津大學與歐洲阿斯利康製藥公司(AstraZeneca Plc)合作研發的一種新冠肺炎疫苗,在進行測試期間有一名在英國參與測試的志願者出現無法解釋的疾病及有嚴重的不良反應。阿斯利康周二證實,已經暫停了測試計畫。
即時未知道那款潛在疫苗出現甚麼性質的安全問題,也不知道是甚麼時候出現問題,但預料該名志願者可以康復,不會有生命危險。
阿斯利康發言人發表聲明稱,工作人員進行標準檢視時,啟動了暫停進行疫苗測試的機制,藉以研究相關的安全數據。
阿斯利康是與英國牛津大學合作研發疫苗,並在美國、英國不同地點展開後期測試。消息人士透露,一名在英國參與測試計畫的志願者,身體出現問題。

阿斯利康是與英國牛津大學合作研發疫苗。AP圖片
牛津大學與英國藥廠阿斯利康共同研發的疫苗名為「ChAdOx1 nCoV-19」,這個項目進展超出預期,在7月20日在世界頂級醫學期刊《刺針》上公布第2期臨床結果時,曾經令人十分鼓舞。
牛津大學的科學家將一種可以導致黑猩猩感冒的病毒進行基因工程改造,加上新冠病毒的基因,使其不會致人傳染,但「看」上去更像新冠病毒,然後用腺病毒為載體,將這些新冠病毒基因帶入人體,引發免疫反應,讓免疫系統學習如何攻擊新冠病毒,產生應對新冠病毒的T細胞。
目前針對新冠病毒的幾乎都聚焦於抗體,但抗體只是人類免疫系統的一部分,T細胞對於免疫同樣重要。幾乎所有的有效疫苗都會在誘發抗體反應的同時誘發T細胞產生反應。抗體可以使新冠病毒失去效力,而T細胞則是一種白細胞,有助於協調免疫系統,可以發現人體內哪些細胞已被病毒感染並摧毀這些細胞。
但上述這種「腺病毒載體疫苖」策略,過去應用相對有限,在對付流感或肺炎病毒方面,僅限於在科學的範疇內的實驗。
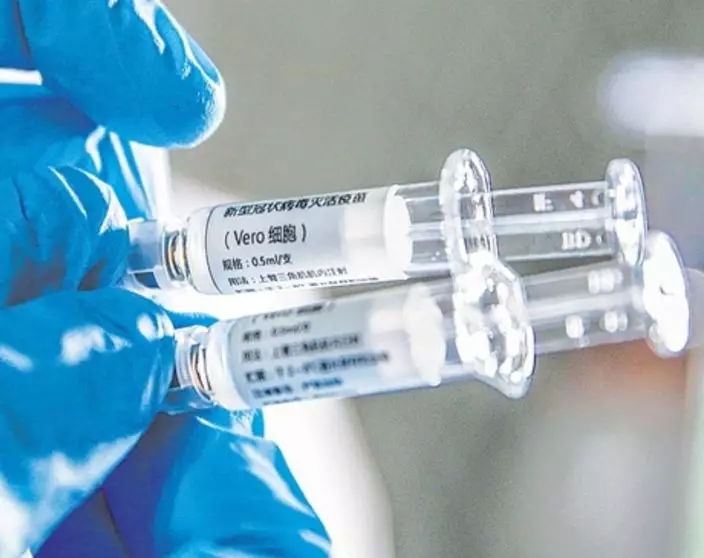
圖: 中國工作人員在展示首批獲得臨床研究批件的新冠病毒滅活疫苗。新華社圖片
其實新冠疫苖有5種路徑:
1. 全病毒滅活疫苗,這是最傳統做疫苖的方法,即是把將病原微生物殺死後,保留整個微生物體,做成疫苗。很多疫苖都是這樣做的,如甲型肝炎滅活疫苗、日本腦炎滅活疫苗、小兒麻痺滅活疫苗、流感(全病毒)疫苗等。中國部份疫苖用這種傳統做法,例如國藥集團旗下的中國生物武漢生物制品研究所,研發的就是滅活疫苗,是全球首個獲得臨牀試驗批准的新冠病毒滅活疫苗。這種傳統好處是安全副作用少,但壞處是抗疫效用可能不夠持久。

圖: 工作人員在國藥中國生物新冠疫苗生産基地質量檢定部門,從傳遞窗拿取新型冠狀病毒滅活疫苗樣品。新華社圖片
2. 重組蛋白疫苗,是通過基因工程,化學分解或有控制性的蛋白質水解方法,提取新冠病毒最有可能作為抗原的S蛋白,把它注射到人體,刺激人體産生抗體。相當於不生産完整病毒,而是單獨生産很多新冠病毒的關鍵部件「鑰匙」,將其交給人體的免疫係統認識,然後學習去對抗新冠病毒。中國已掌握了大規模生産高質量和高純度疫苗蛋白的技術,這是一條可以大規模快速生産疫苗的技術路線。重組蛋白疫苗相對全病毒疫苗來講,重組蛋白疫苗安全性更高,穩定性更好。免疫具有持久性,一次接種可獲得長期免疫力,無需反覆多次加強免疫。
3. 腺病毒載體疫苗(就是上述牛津疫苖的做法),是採用基因工程方法,用腺病毒作為載體,把新冠病毒中有保護性作用的S蛋白轉到腺病毒裡面去,做出以腺病毒為載體的重組疫苗,打入人體,刺激人體免疫反應。
這種技術並非全新,相對成熟,曾被用來研發出埃博拉病毒疫苗,不過也有研究發現腺病毒載體疫苗的成功率無法完全保證,因為重組病毒載體疫苗研發需要考慮如何克服「預存免疫」問題。以進入臨床試驗的重組新冠疫苗為例,該疫苗以5型腺病毒作載體,但絕大多數人成長過程中曾感染過5型腺病毒,體內可能存在能中和腺病毒載體的抗體,從而可能攻擊載體、降低疫苗效果。也就是説,疫苗的安全性較高,但有效性可能不足。不過今次牛津疫苖出現的偏偏是安全性問題。
香港上市公司康希諾公司和中國軍科院軍事醫學研究所陳薇團隊的合作疫苖,也和牛津大學的路徑一樣,用腺病毒載體的方法。同一個團隊過去自主研制的重組埃博拉病毒病疫苗,也是用腺病毒作載體。
而深圳免疫基因治療研究院的兩支候選疫苗,一種是慢病毒載體修飾樹突狀細胞疫苗,另一是慢病毒載體修飾的具病原特異性的人工抗原提呈細胞疫苖,也是病毒載體疫苖。
4. 核酸疫苗。核酸疫苗包括mRNA疫苗和DNA疫苗,是將新冠病毒中有保護性作用的編碼S蛋白的基因,mRNA或者DNA直接注入人體,利用人體細胞在人體內合成S蛋白,刺激人體産生抗體。通俗的説,相當于把一份記錄詳細的病毒檔案交給人體的免疫係統。美國生物醫藥新創公司Moderna正進行第3期臨床試驗的mRNA新冠疫苗,就屬于核酸疫苗。另一家美國生物製藥公司Inovio在聖地亞哥的實驗室研發的INO-4800疫苖,就是基於DNA開發的新冠核酸疫苗。
核酸疫苗的優點是:研制時不需要合成蛋白質或病毒,流程簡單。核酸疫苗是全世界都在積極探索的疫苗新技術,目前全球還沒有核酸疫苗上市。中國一些高校正開展這條路線的研究。
美國這兩款率先進入臨牀試驗的新冠疫苗都沒有遵循傳統,而是另闢蹊徑,採用了基因改造和編輯技術。這種技術的最大優勢是快速、便捷,只要有病毒基因序列,就能快速改造抗原。Moderna公司的mRNA-1273疫苗從新冠病毒基因序列公布到開時臨牀試驗只用了3個月,INO-4800的設計只用了3小時。
但這種疫苗的技術太新了,還沒有成功先例,所以也不知道研發過程中前方哪裏可能有問題。從産業角度看,雖然其生産工藝本身並不複雜,但全球多數國家該領域基礎比較薄弱,尚未形成穩定可控的大規模生産供應鏈。所以它的缺點是:無成功先例,多數國家無法大規模生産,可能因價格較貴,而難以普及到低收入國家。而且由於是全新技術,也怕有新的安全性問題,但其有效性應該較高。
美國Moderna公司在mRNA疫苗研製領域走在全球最前列,該公司研製的其他多種同類型疫苗也進行過一期臨床,但後面的臨床測試都沒做。所以從它的安全性、長期效果、生產量產方面來看,還不知道今後會遇到怎樣的問題。
5. 減毒流感病毒載體疫苗。減毒流感病毒載體疫苗是用已批準上市的減毒流感病毒疫苗作為載體,攜帶新冠病毒的S蛋白,共同刺激人體産生針對兩種病毒的抗體。簡單地説,這種疫苗就是低毒性流感病毒戴上新冠病毒S蛋白「帽子」後形成的融合病毒,可以一石二鳥,既能防流感又能防新冠。在新冠肺炎與流感流行重疊時,其臨床意義非常大。由於減毒流感病毒容易感染鼻腔,所以這種疫苗僅通過滴鼻的方式就可以完成疫苗接種。
病毒減毒活疫苗是非常重要的一類疫苗,我們平時常見的減毒活疫苗有:乙型腦炎減毒活疫苗、甲型肝炎減毒活疫苗、麻疹減毒活疫苗等。但減毒活疫苗的缺點是:研發過程漫長。
總括而言,中國進入臨牀試驗頭5種疫苗,其中3種基於病毒載體技術,另外2種爲傳統滅活疫苗。從疫苗研發技術來看,滅活疫苗是最傳統的研發路徑,在體外培養新冠病毒後滅活,但仍能刺激人體免疫系統產生抗體。其優點在於製備簡單快速,安全性較高。但也有接種劑量大,免疫期短等不足,最大的缺點是可能引起抗體增強效應,增強病毒在體內的複製,引發嚴重疾病等不良反應。
相比而言,載體疫苗技術也比較成熟,優點在於安全性高,引發的不良反應少,但缺點在於如果人體曾感染過載體病毒,體內存在抗體,則可能攻擊疫苗載體,降低疫苗有效性。如今牛津測試出事,亦令人對「腺病毒載體」方法存疑。
美國搞的核酸疫苗另闢蹊徑,大大加速了研發進程,並且疫苗有良好的耐受性,可以引發對病原的持久免疫反應。但由於核酸疫苗研發技術尚處於早期階段,有許多未知的困難。
深喉
** 博客文章文責自負,不代表本公司立場 **